"熬的不是夜,是'偷來'的短暫自由""白天歸順于生活,晚上臣服于靈魂"—— 千千萬萬"守零人"的內(nèi)心獨白!
線粒體:哈?人!關(guān)掉你的網(wǎng)抑云,我要裂了......
Section.01
人為什么會睡覺?
你有沒有想過,我們?yōu)槭裁磿X? 我指的是......不受控的,打瞌睡。無論你憑借意志陪月亮熬到凌晨幾點,終有一個瞬間閉眼投降。緊跟著的便是熬夜過后身體的種種不良反應(yīng),讓你感覺身體被掏空,下一秒就要見到老天奶。。。
其實從進(jìn)化的角度看,睡眠并不是件好事。因為如果生物體長時間無法感知和與環(huán)境互動,可能會增加被捕食的風(fēng)險。但神奇的是!從秀麗隱桿線蟲的簡單神經(jīng)系統(tǒng),一直到人類大腦,睡眠從未被進(jìn)化掉?![1]。
于是,科學(xué)家們將睡眠稱之為一種非常特殊的現(xiàn)象。加之睡眠不足會帶來認(rèn)知能力受損、代謝功能障礙、患病風(fēng)險增加,甚至?xí)?dǎo)致死亡等有害影響。So,睡眠,既是動物界最常見的行為之一,也是自然界最大的謎團(tuán)之一。
你可能要說了,存在即合理嘛~ 哎嘿!兄弟,它不僅合理,還有規(guī)律——生物鐘。
生物鐘,又稱晝夜節(jié)律 (Circadian rhythm):是一種生理現(xiàn)象,以內(nèi)源性、持續(xù)的,呈現(xiàn)以約 24 小時為周期的變動。
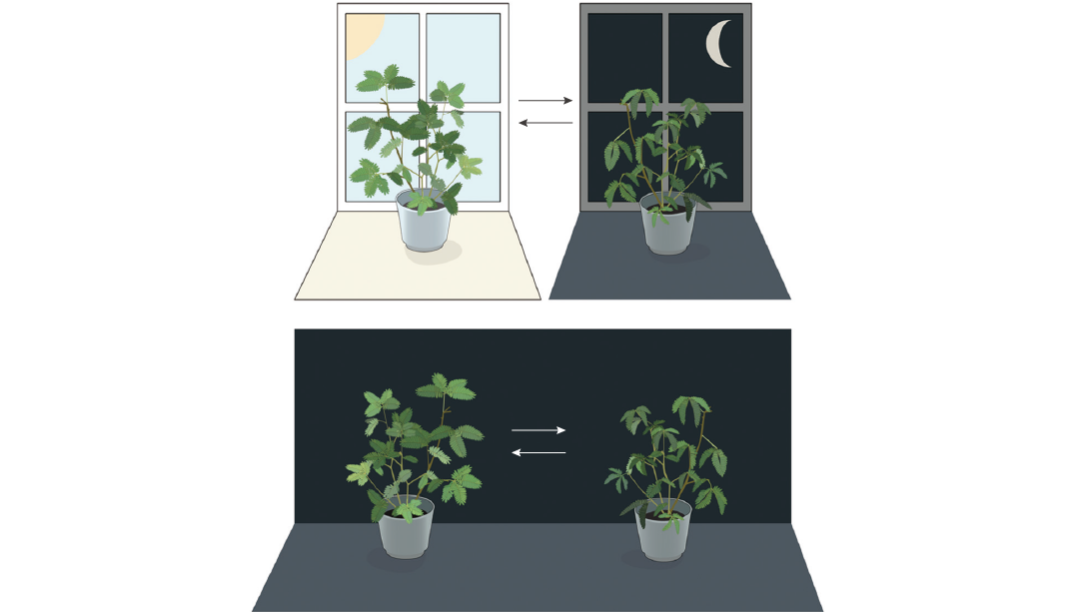
圖 1. 含羞草的葉片白天張開,黃昏時閉合。且當(dāng)含羞草處于持續(xù)黑暗中時,其葉片仍會維持正常的晝夜節(jié)律[2]。
科學(xué)家成功克隆了 "周期" 基因 period,period 基因的編碼蛋白 PER 夜間積累,白天降解,其蛋白水平的 24 h 周期性波動與晝夜節(jié)律同步。TIM 蛋白可以與 PER 蛋白結(jié)合,攜帶后者進(jìn)入細(xì)胞核,通過抑制 period 基因活性來完成負(fù)反饋調(diào)控,減少自身蛋白的合成。此外,基因 doubletime 編碼的蛋白 DBT 可以延緩 PER 蛋白的積累,使后者的震蕩頻率基本吻合 24 h 周期 (圖 2)。

圖 2. period 基因負(fù)反饋調(diào)控環(huán)路[2]。
2017 年的諾貝爾生理學(xué)或醫(yī)學(xué)獎也讓果蠅這一卓爾不凡的小動物再次身顯名揚,這也是第五座因果蠅而獲得的諾獎。后續(xù)小 M 會位大家專門出一期關(guān)于實驗中常見模式生物的文章,小伙伴們可以淺淺關(guān)注一下~

言歸正傳!果蠅,作為研究睡眠相當(dāng)有用的動物模型[3]。研究發(fā)現(xiàn),在其睡眠調(diào)節(jié)神經(jīng)回路中,背側(cè)扇形體 (dorsal fan-shaped body, dFB/dFNBs) 是主要的促進(jìn)睡眠區(qū)域[4]。更為神奇的是,近期 Nature 發(fā)表的研究性論文發(fā)現(xiàn),睡眠與線粒體緊密相關(guān)——當(dāng)在背側(cè)扇狀體 (dFBNs) 中檢測到過多的線粒體損傷時,就會觸發(fā)睡眠。
Section.02
Nature 發(fā)文:
線粒體起源的睡眠壓力
2025 年 7 月 16 日,Nature 發(fā)表標(biāo)題為“Mitochondrial origins of the pressure to sleep”的研究性論文,該論文研究了睡眠壓力 (sleep pressure) 的線粒體起源,探討了大腦中分子變化與睡眠需求的關(guān)聯(lián)[5]。
線粒體基因表達(dá)上調(diào)
首先,研究人員通過分析休息和睡眠剝奪的果蠅的單細(xì)胞轉(zhuǎn)錄組,發(fā)現(xiàn)在睡眠剝奪后,上調(diào)的轉(zhuǎn)錄本主要在投射到背側(cè)扇狀體 (dFBNs) 的睡眠控制神經(jīng)元中表達(dá),且在 dFBN 中上調(diào)的轉(zhuǎn)錄本,幾乎只編碼參與線粒體呼吸和 ATP 合成的蛋白質(zhì) (圖 3a)。
如圖所示,通過對 12 小時夜間睡眠剝奪后 dFBN 中水平發(fā)生變化的 122 個轉(zhuǎn)錄本進(jìn)行基因本體分析,發(fā)現(xiàn)睡眠剝奪導(dǎo)致編碼電子傳遞復(fù)合物 I-IV、ATP 合酶 (復(fù)合物 V)、ATP-ADP 載體 sesB 和三羧酸循環(huán)酶 (檸檬酸合酶 kdn、琥珀酸脫氫酶 B 亞基和蘋果酸脫氫酶 Men-b) 成分的轉(zhuǎn)錄本選擇性上調(diào),而參與突觸組裝、突觸囊泡釋放和突觸前穩(wěn)態(tài)可塑性的基因產(chǎn)物則選擇性下調(diào)。
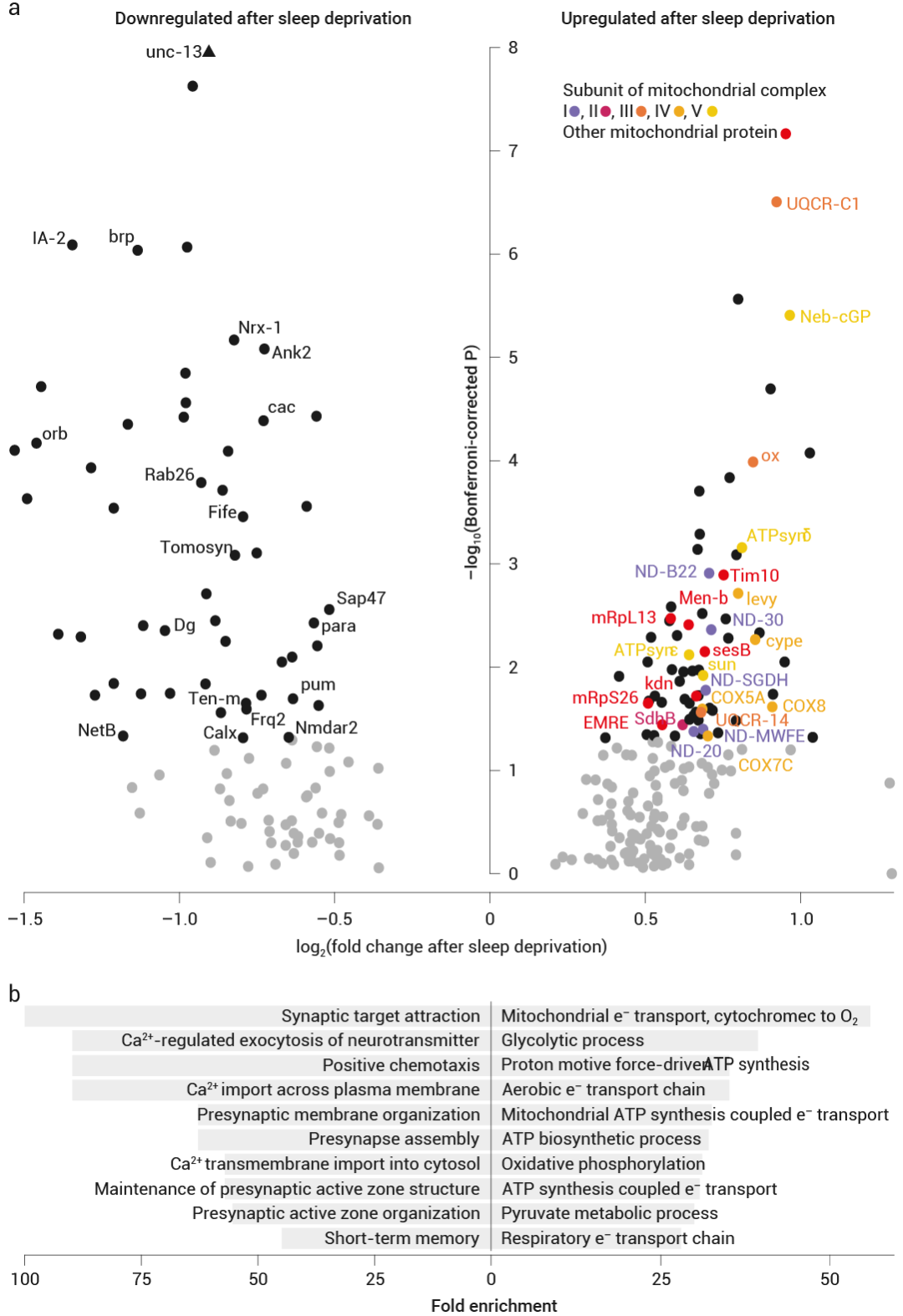
睡眠剝奪 — 線粒體: 不睡么? 我要 "裂" 了
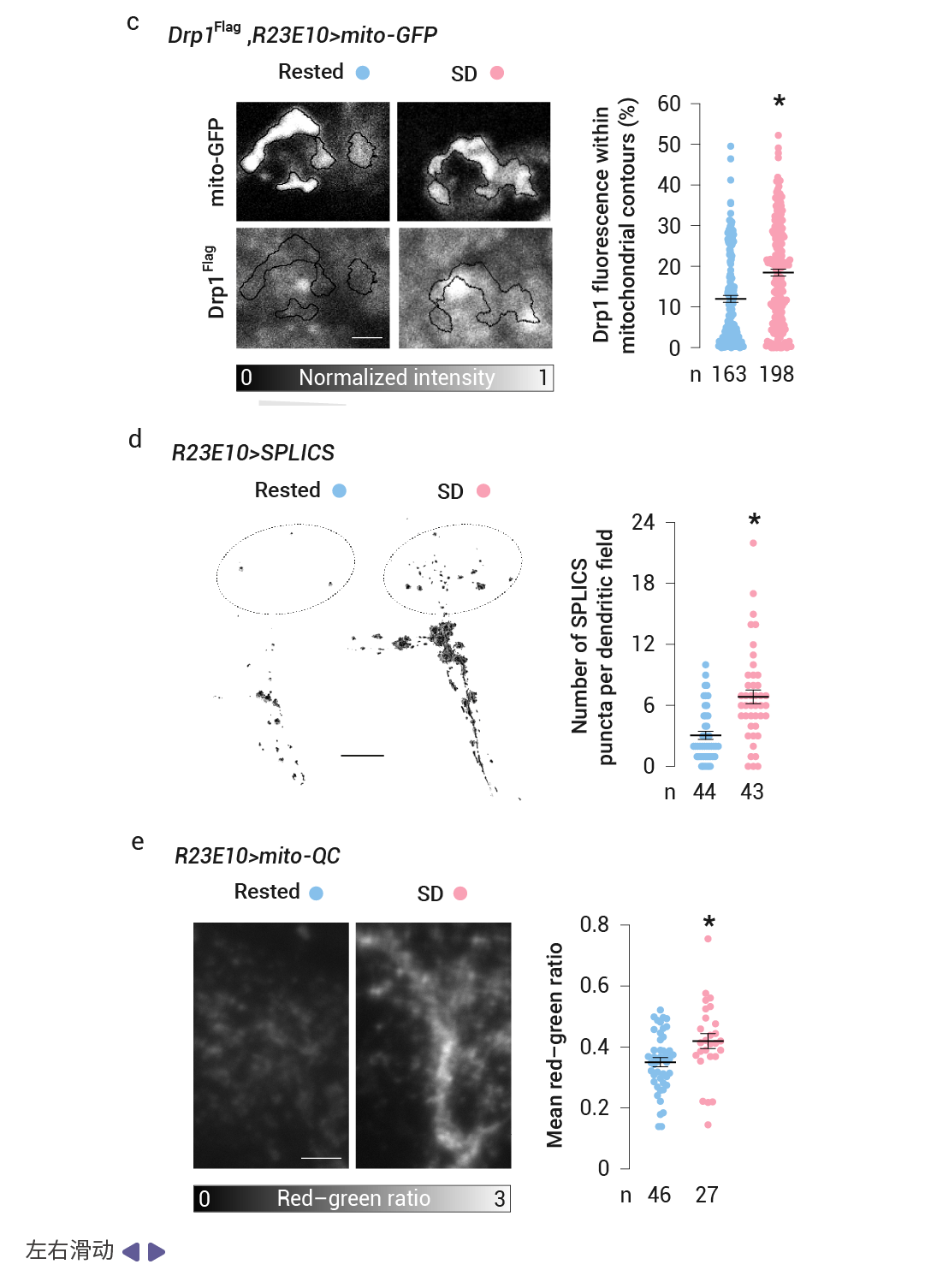
作者用基質(zhì)定位的綠色熒光蛋白 (mito-GFP) 標(biāo)記了 dFBN 的線粒體,并在一系列獨立的實驗中,用共聚焦激光掃描顯微鏡 (CLSM) 或光學(xué)光子重排顯微鏡 (OPRM) 對神經(jīng)元的樹突區(qū)進(jìn)行成像。發(fā)現(xiàn)睡眠剝奪后的基因表達(dá)變化伴隨著線粒體碎片化、線粒體自噬增強以及線粒體與內(nèi)質(zhì)網(wǎng)之間接觸數(shù)量的增加,恢復(fù)睡眠后,形態(tài)變化是可逆的。
首先,在線粒體形態(tài)上,研究發(fā)現(xiàn)無論是機械攪拌還是人為提高多巴胺水平所致的睡眠剝奪,都會導(dǎo)致 dFBN s 中線粒體的尺寸縮小、伸長率降低、分支減少 (圖 4a-b)。并導(dǎo)致動力蛋白相關(guān)蛋白 1 (Drp1) (外膜的關(guān)鍵裂變動力蛋白) 從細(xì)胞質(zhì)移位到線粒體表面 (圖 4c),OPRM 檢測到線粒體數(shù)量的伴隨增加 (圖 4b),表明線粒體發(fā)生分裂。同時,睡眠剝奪的果蠅的 dFBN 中接觸位點計數(shù)較高,也就是說睡眠剝奪導(dǎo)致 dFBN 中線粒體-內(nèi)質(zhì)網(wǎng)接觸更加豐富,從而形成補充過氧化脂質(zhì)的通道 (圖 4d)。同時,mito-QC (一種檢測線粒體進(jìn)入酸性自噬溶酶體的比例傳感器) 則報告了線粒體自噬增強 (圖 4e)。而在隨后的恢復(fù)睡眠期間,線粒體的增殖和融合導(dǎo)致它們的體積、形狀和分支長度反彈至基線值以上 (圖 4a-b)。這表明線粒體損傷可能會引發(fā)睡眠沖動。
此外,利用基因編碼的 ATP 傳感器 iATPSnFR 和 ATeam 進(jìn)行的測量表明,一夜睡眠剝奪后,dFBN 中的 ATP 濃度比靜息狀態(tài)下高出約 1.2 倍。而當(dāng) dFBN 本身受到刺激 (模擬睡眠) 時,ATP 濃度會降至基線以下,這是由于 dFBN 去極化會增加 Na+-K+ 泵的 ATP 消耗,從而減少電子向 ROS 的轉(zhuǎn)移 (圖 5),這保留了其線粒體的形態(tài)。

線粒體:裂變—睡的少,融合—叫不醒
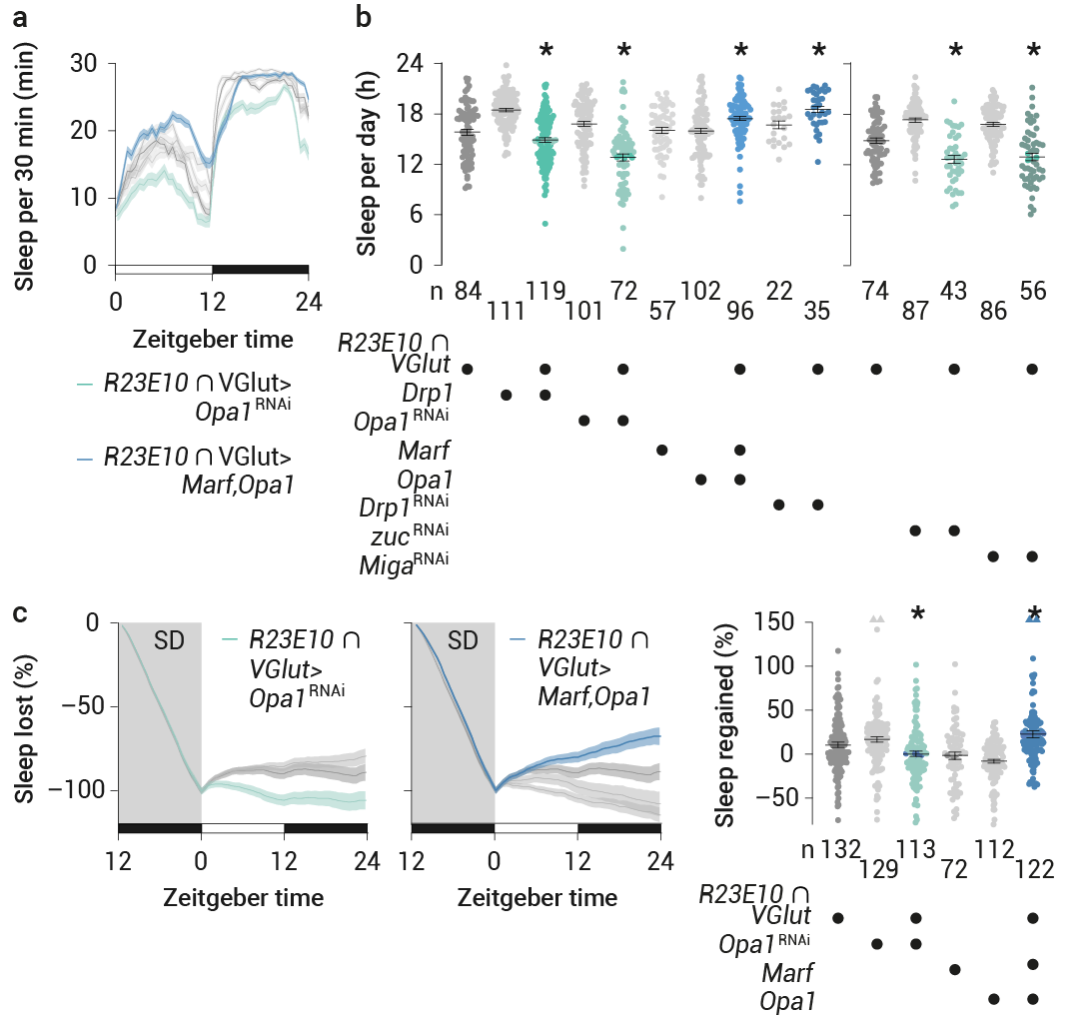
隨后,作者人為地人為控制了線粒體的裂變和融合。因為如果線粒體裂變和融合之間平衡的變化是反饋機制的一部分。那么在 dFBN 中實驗性地誘導(dǎo)這些穩(wěn)態(tài)反應(yīng)應(yīng)該會改變睡眠的設(shè)定點:線粒體的分裂預(yù)計會減少睡眠時間和深度,而反之線粒體融合預(yù)計會增加睡眠時長和深度。
于是,作者對在線粒體動力學(xué)中具有中心調(diào)控作用的三種 GTP 酶進(jìn)行了實驗控制 (圖 4a):(1) 裂變動力蛋白 Drp1,以及內(nèi)外線粒體膜的整合蛋白 (2) 視神經(jīng)受損 1 (Opa1) 和 (3) 線粒體融合蛋白子 (Marf) (它們在順式和反式的聚合使得相應(yīng)的膜融合)。

通過過表達(dá) Drp1 或 RNAi 介導(dǎo)的 Opa1 減少 (在較小程度上也包括 Marf) 來使 dFBN 線粒體碎片化,減少了睡眠 (圖 7a-b)。消除對睡眠剝奪的穩(wěn)態(tài)反應(yīng) (圖 7c),并且無論睡眠史如何,均降低了 dFBN 中的 ATP 濃度。
將平衡傾向于線粒體融合則產(chǎn)生了相反的效果:在 dFBN 中敲低 Drp1 或過表達(dá) Opa1 加 Marf——或者單獨過表達(dá) Opa1,但不包括單獨過表達(dá) Marf——增加了基線及反彈睡眠 (圖 7a-c),并提高了覺醒閾值,且不會引起過表達(dá)偽影或明顯的發(fā)育缺陷。
同時,當(dāng)這些干預(yù)針對投射神經(jīng)元或 Kenyon 細(xì)胞時,沒有改變睡眠。報道顯示,在泛神經(jīng)元或膠質(zhì)細(xì)胞 RNAi 敲低 Drp1 或 Marf 基因后,睡眠喪失現(xiàn)象普遍存在。在 dFBN 中,Drp1 或 Marf 基因的表達(dá)會雙向改變睡眠 (圖 7a-c)。
最后,作者提到睡眠可能是為了滿足代謝需求而進(jìn)化的。比如,線粒體融合后,AgRP 神經(jīng)元的電輸出會增加,從而促進(jìn)體重增加和脂肪沉積;這就像線粒體融合后 dFBN 的電輸出會增加以促進(jìn)睡眠一樣。刪除 AgRP 神經(jīng)元中的線粒體融合蛋白會損害食物攝入,就像干擾 dFBN 中的線粒體融合會損害睡眠誘導(dǎo)一樣。這些相似之處表明,睡眠壓力和饑餓感都源自線粒體,并且電子會流經(jīng)各自反饋控制器的呼吸鏈,就像沙漏中的沙子一樣,決定何時需要恢復(fù)平衡。
Section.03
小結(jié)
總之,當(dāng)你遲遲不睡時,你的線粒體先“破大防”,碎片化線粒體增加,線粒體自噬增強,并頻繁“聯(lián)系”內(nèi)質(zhì)網(wǎng),種種損傷只為喚起你的睡眠沖動,從而促使睡眠!當(dāng)然,線粒體這些形態(tài)學(xué)變化在恢復(fù)睡眠后是可逆的,并且由于呼吸鏈中電子溢出的增加而減弱 (電子過剩誘導(dǎo)睡眠)。此外,誘導(dǎo)或抑制 dFBN 中的線粒體裂變或融合,會以相反的方向改變睡眠和睡眠控制細(xì)胞的電特性:線粒體融合增加睡眠,而碎片化的線粒體減少睡眠。睡眠,像衰老一樣,可能是有氧代謝不可避免的結(jié)果。
產(chǎn)品推薦
Mdivi-1 (HY-15886)
是選擇性的發(fā)動蛋白相關(guān)蛋白 1 (Drp1) 抑制劑。Mdivi-1 是一種有效的線粒體分裂/線粒體自噬 (mitophagy) 抑制劑。
MFI8 (HY-150031)
是一種線粒體融合 (mitochondrial fusion) 的小分子抑制劑。
MitoTracker Deep Red/ MitoTracker Green (HY-D1783)
線粒體紅色/綠色熒光探針。
JC-1 (HY-15534)
是一種廣泛用于檢測線粒體膜電位的理想熒光探針。正常線粒體內(nèi),JC-1 聚集在線粒體基質(zhì)中形成聚合物,聚合物發(fā)出強烈的紅色熒光 (Ex=585 nm, Em=590 nm) ;在線粒體膜電位較低時,JC-1不能聚集在線粒體的基質(zhì)中,產(chǎn)生綠色熒光 (Ex=510 nm, Em=527 nm) 。
TPE-PY (HY-D2639)
是一種針對線粒體的熒光染料,能特異性靶向線粒體。TPE-PY 主要用于生物成像領(lǐng)域,特別是活細(xì)胞中線粒體的特異性染色研究,有助于觀察線粒體的位置、形態(tài)和數(shù)量。

[1] Ly S, Pack AI, Naidoo N. The neurobiological basis of sleep: Insights from Drosophila. Neurosci Biobehav Rev. 2018 Apr;87:67-86.
[2] 2017年度諾貝爾生理學(xué)或醫(yī)學(xué)獎, 生命科學(xué), 2017 年 12 月, 第 29 卷 第 12 期, DOI: 10.13376/j.cbls/2017161
[3] Tainton-Heap LAL, et al. A Paradoxical Kind of Sleep in Drosophila melanogaster. Curr Biol. 2021 Feb 8;31(3):578-590.e6.
[4] Kato YS,et al. Interneurons of fan-shaped body promote arousal in Drosophila. PLoS One. 2022 Nov 21;17(11):e0277918.
[5] Kato YS, et al. Interneurons of fan-shaped body promote arousal in Drosophila. PLoS One. 2022 Nov 21;17(11):e0277918.

相關(guān)產(chǎn)品
免責(zé)聲明
- 凡本網(wǎng)注明“來源:化工儀器網(wǎng)”的所有作品,均為浙江興旺寶明通網(wǎng)絡(luò)有限公司-化工儀器網(wǎng)合法擁有版權(quán)或有權(quán)使用的作品,未經(jīng)本網(wǎng)授權(quán)不得轉(zhuǎn)載、摘編或利用其它方式使用上述作品。已經(jīng)本網(wǎng)授權(quán)使用作品的,應(yīng)在授權(quán)范圍內(nèi)使用,并注明“來源:化工儀器網(wǎng)”。違反上述聲明者,本網(wǎng)將追究其相關(guān)法律責(zé)任。
- 本網(wǎng)轉(zhuǎn)載并注明自其他來源(非化工儀器網(wǎng))的作品,目的在于傳遞更多信息,并不代表本網(wǎng)贊同其觀點和對其真實性負(fù)責(zé),不承擔(dān)此類作品侵權(quán)行為的直接責(zé)任及連帶責(zé)任。其他媒體、網(wǎng)站或個人從本網(wǎng)轉(zhuǎn)載時,必須保留本網(wǎng)注明的作品第一來源,并自負(fù)版權(quán)等法律責(zé)任。
- 如涉及作品內(nèi)容、版權(quán)等問題,請在作品發(fā)表之日起一周內(nèi)與本網(wǎng)聯(lián)系,否則視為放棄相關(guān)權(quán)利。
 手機版
手機版 化工儀器網(wǎng)手機版
化工儀器網(wǎng)手機版
 化工儀器網(wǎng)小程序
化工儀器網(wǎng)小程序
 官方微信
官方微信 公眾號:chem17
公眾號:chem17
 掃碼關(guān)注視頻號
掃碼關(guān)注視頻號

















 采購中心
采購中心